мқҙлӢӨкёҲ newsmedical@daum.net
мӢқн’Ҳмқҳм•Ҫн’Ҳм•Ҳм „мІҳ(мІҳмһҘ лҘҳмҳҒ진) мӢқн’Ҳмқҳм•Ҫн’Ҳм•Ҳм „нҸүк°Җмӣҗмқҙ мһҗмІҙ к°ңл°ңн•ң вҖҳн”јл¶Җк°җмһ‘м„ұ мӢңн—ҳвҖҷмқҙ м ң30м°Ё вҖҳOECD көӯк°ҖмӢңн—ҳм§Җм№Ён”„лЎңк·ёлһЁмЎ°м •мһҗ мһ‘м—…л°ҳ нҡҢмқҳ(WNT)вҖҷм—җм„ң OECDмқҳ лҸ…м„ұмӢңн—ҳ к°Җмқҙл“ңлқјмқёмңјлЎң мҠ№мқёлҗҗлӢӨкі м§ҖлӮң 4мқј л°қнҳ”лӢӨ.
мқҙлІҲм—җ мҠ№мқёл°ӣмқҖ к°Җмқҙл“ңлқјмқёмқҖ н”јл¶Җм—җ л°”лҘҙлҠ” нҷ”мһҘн’Ҳ л“ұмқҳ к°ңл°ңВ·мӢңн—ҳм—җ нҷңмҡ©лҗҳлҠ” мӢңн—ҳл°©лІ•мқҙл©°, н”јл¶Җк°җмһ‘м„ұ мӢңн—ҳмңјлЎңлҠ” лҜёкөӯВ·мң лҹҪВ·мқјліём—җ мқҙм–ҙ 4лІҲм§ёлЎң OECD мҠ№мқёмқ„ л°ӣм•ҳлӢӨ.
мқҙ мӢңн—ҳлІ• к°Җмқҙл“ңлқјмқёмқҖ OECD мқҙмӮ¬нҡҢлҘј кұ°міҗ кіөн‘ңлҗң нӣ„ м„ёкі„ к°Ғкөӯмқҳ к·ңм ңкё°кҙҖм—җ м ңм¶ңлҗҳлҠ” лҸ…м„ұмӢңн—ҳм—җ нҷңмҡ©лҗ мҳҲм •мқҙлӢӨ.
мӢқм•ҪмІҳк°Җ к°ңл°ңн•ң н”јл¶Җк°җмһ‘м„ұ мӢңн—ҳмқҖ вҖҳмң м„ёнҸ¬л¶„м„қмқ„ мқҙмҡ©н•ң көӯмҶҢлҰјн”„м ҲмӢңн—ҳлІ•вҖҷмңјлЎң лӢӨлҘё н”јл¶Җк°җмһ‘м„ұ мӢңн—ҳлІ•кіј лӢ¬лҰ¬ лҸҷл¬јм—җм„ң лҰјн”„м Ҳмқ„ мұ„м·Ён•ҳм—¬ н”јл¶Җк°җмһ‘ л“ұмқҳ л©ҙм—ӯл°ҳмқ‘ м§Җн‘ңлҘј 추к°ҖлЎң нҷ•мқён• мҲҳ мһҲм–ҙ кё°мЎҙм—җ к°ңл°ңлҗң вҖҳн”јл¶Җк°җмһ‘м„ұ мӢңн—ҳвҖҷліҙлӢӨ м •нҷ•лҸ„к°Җ лҶ’мқҖ л°©лІ•мқҙлӢӨ.
лҳҗ лҸҷл¬ј(кё°лӢҲн”Ҫ)м—җ нҷҚл°ҳВ·л¶Җмў… л“ұ м—јмҰқмқ„ мң л°ңн•ҳлҠ” кё°мЎҙ нҸүк°Җл°©мӢқ ліҙлӢӨ мӢңн—ҳкё°к°„мқҙ 3분мқҳ 1мҲҳмӨҖмңјлЎң лҸҷл¬ј кі нҶөкіј мӮ¬мҡ© к°ңмҲҳк°Җ к°җмҶҢлҗҳл©°, мӢӨн—ҳм—җ мӮ¬мҡ©лҗҳлҠ” вҖҳBALC/c л§Ҳмҡ°мҠӨвҖҷлҠ” көӯлӮҙ мғқмӮ°мқҙ к°ҖлҠҘн•ҙ 비мҡ©мқҙ м Җл ҙн•ҳкі мүҪкІҢ кө¬мһ…н• мҲҳ мһҲлҠ” мһҘм җмқҙ мһҲлӢӨ.
м•Ҳм „нҸүк°Җмӣҗ нҠ№мҲҳлҸ…м„ұкіјкіј лҸ…м„ұм—°кө¬кіјлҠ” вҖңмқҙлІҲ OECDмқҳ лҸ…м„ұмӢңн—ҳ к°Җмқҙл“ңлқјмқё мұ„нғқмңјлЎң лҸ…м„ұмӢңн—ҳ к°Җмқҙл“ңлқјмқё к°ңл°ң көӯк°ҖлЎңм„ң көӯм ң мң„мғҒ м ңкі м—җ кё°м—¬н• кІғмңјлЎң кё°лҢҖн•ңлӢӨвҖқкі л°қнҳ”лӢӨ.
н•ңнҺё мӢқм•ҪмІҳк°Җ к°ңл°ңн•ң вҖҳмқёмІҙк°Ғл§ү лӘЁлҚёмқ„ мқҙмҡ©н•ң м•Ҳмһҗк·№ лҸҷл¬јлҢҖмІҙмӢңн—ҳлІ•вҖҷмқҙ OECD мӢ к·ң н”„лЎңм қнҠёлЎң м§ҖлӮң 4мӣ” мұ„нғқлҗҗмңјл©°, н–Ҙнӣ„ көӯм ң м „л¬ёк°Җл“Өмқҳ нҸүк°ҖлҘј кұ°міҗ OECD м „л¬ёк°Җ нҡҢмқҳм—җм„ң к°Җмқҙл“ңлқјмқёмқ„ кІҖнҶ н• мҳҲм •мқҙлӢӨ.
- TAG



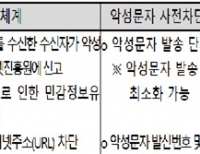 м•…м„ұл¬ёмһҗ мӮ¬м „м°ЁлӢЁ м„ң비мҠӨ мӢңлІ” мҡҙмҳҒ
м•…м„ұл¬ёмһҗ мӮ¬м „м°ЁлӢЁ м„ң비мҠӨ мӢңлІ” мҡҙмҳҒ
 [м„ұнҳ•мҷёкіј мӢңмҲ м ңлҢҖлЎң м•Ңкё°] л’ӨнҠёмһ„ ліөмӣҗ л°Ҹ л°‘нҠёмһ„ ліөмӣҗ мӢң кі л Өн•ҙм•ј н• мЈјмқҳмӮ¬н•ӯмқҖ?
[м„ұнҳ•мҷёкіј мӢңмҲ м ңлҢҖлЎң м•Ңкё°] л’ӨнҠёмһ„ ліөмӣҗ л°Ҹ л°‘нҠёмһ„ ліөмӣҗ мӢң кі л Өн•ҙм•ј н• мЈјмқҳмӮ¬н•ӯмқҖ?