식품의약품안전처(처장 오유경)가 4월 1일부터 ‘해외제조업소 차등 등록제’를 10월 31일까지 시범적으로 운영한다.
◆올해 시범 운영 대상 품목
올해 시범 운영 대상 품목은 작년에 수행한 연구사업에서 도출된 위해 우려 품목(건강기능식품, 농산가공식품류, 조미식품) 중 부적합률이 높고, 미국‧일본 등 주요 수출국에서 제품 생산 시 우수제조시설(GMP) 등 식품안전관리시스템을 적용토록 해 인증서 확보에 국내 수입자의 부담이 적은 건강기능식품이다.
식약처는 건강기능식품 해외제조업소를 대상으로 한 시범 운영 결과를 검토해 향후 단계적으로 차등 등록 대상 품목을 확대한다는 계획이다.
건강기능식품 수입자 등은 해외제조업소 등록 시 수출국 정부 또는 국제적으로 공인된 인증서를 제출해야 하며, 제출 가능한 인증서의 종류는 수입식품정보마루 누리집에서 확인할 수 있다.
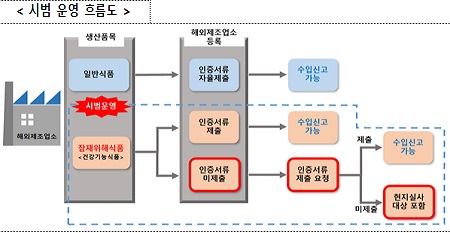
시범사업 운영 기간 중에는 인증서 제출 없이도 해외제조업소 등록은 가능하다. 하지만 식약처는 해당 업소를 차년도 현지실사 대상으로 포함해 관리한다는 계획이다.
◆ ‘해외제조업소 차등 등록 민원 안내서’ 제작·배포
식약처는 ‘해외제조업소 차등 등록제’에 대해 수입자와 해외제조업소 설치·운영자의 이해도를 높이고, 시범 운영 사업의 원활한 추진을 위해 ‘해외제조업소 차등 등록 민원 안내서’를 제작·배포한다.
이번 안내서에는 건강기능식품 해외제조업소 등록 시 수입자 등이 준비해야 하는 ▲식품안전관리 인증서의 종류 ▲시스템 등록 방법 ▲주요 질의응답 등을 자세히 수록했다.
특히 적극행정의 일환으로 사전에 식품관련 협회, 수입자, 재외국 상공회의소 대상 간담회를 실시해 현장에서 수렴된 의견(국가별 인증 종류, 인증서 샘플 사진 자료, 자세한 Q&A 수록 등 요구)을 안내서에 반영했다.
식약처 수입식품안전정책국 현지실사과는 “앞으로 시범 운영 결과를 토대로 ‘해외제조업소 차등 등록제’의 법적근거를 마련하는 등 제도화에 착수하고 적용 품목을 지속적으로 확대해, 국민이 해외 현지 생산단계에서부터 안전성이 확보된 수입식품을 소비할 수 있도록 최선을 다하겠다”고 밝혔다.
식약처는 수출국 현지 제조단계 안전관리를 보다 강화하기 위해 잠재 위해도(수입통관 검사 부적합 건수, 해외위해정보, 위해성 등에 따라 위해도 분류)가 높은 품목을 생산하는 해외제조업소에 대해 수입자 등이 사전에 해당 업소의 안전관리 체계를 확인하고 식품안전관리시스템 인증서를 제출하도록 하는 ‘해외제조업소 차등 등록제’ 도입을 올해부터 추진한다.
현재 국내로 수입되는 모든 식품 등은 위해도와 관계없이 관계 법령에서 정한 등록 신청서류만 제출하면 해외제조업소 등록이 가능하다.
한편 보다 자세한 내용은 ‘식약처 누리집> 법령/자료 > 법령정보 > 공무원지침서/민원안내서’또는 수입식품정보마루 누리집에서 확인할 수 있고 모바일 E-Book으로도 확인이 가능하다.
[메디컬월드뉴스]
다른 곳에 퍼가실 때는 아래 고유 링크 주소를 출처로 사용해주세요.
 http://www.medicalworldnews.co.kr/news/view.php?idx=1510954300
http://www.medicalworldnews.co.kr/news/view.php?idx=1510954300