명문제약 ‘발사닌정80밀리그램(발사르탄)’이 추가로 판매중지 및 처방 제한됐다.
식품의약품안전처(처장 류영진)가 중국 제지앙 화하이社 ‘발사르탄’에서 ‘N-니트로소디메틸아민(NDMA)’이 검출된 후 국내에 수입 또는 제조되는 모든 ‘발사르탄’ 원료의약품(52개사, 86품목) 대하여 수거·검사를 완료한 결과 이같이 나타났다.
이번 조사로 ‘NDMA’ 잠정 관리 기준(0.3 ppm)을 초과한 ‘발사르탄’ 원료의약품에 대해서는 잠정 판매 및 제조 중지 조치했으며, 해당 원료를 사용하여 제조된 완제의약품에 대해서도 잠정 판매중지하고 처방을 제한하도록 조치했다.
잠정 판매중지 및 처방 제한이 되지 않은 제품들은 ‘NDMA’ 기준에 적합한 제품들로 안전에 큰 문제가 없다는 것이다.
또 향후 국내 유통되는 ‘발사르탄’ 원료의약품과 이를 사용한 완제의약품은 ‘NDMA’ 기준에 적합한 경우에만 공급될 수 있도록 엄격히 관리한다는 방침이다.
◆모든 품목 수거·검사 완료…2개 품목서 ‘NDMA’ 기준 초과 확인
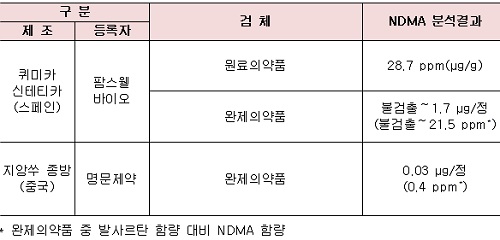
식약처는 지난 8월 6일 41개 품목에 대한 중간조사 결과 발표 후 나머지 ‘발사르탄’ 원료의약품 45개 품목을 수거·검사한 결과, 2개 품목에서 ‘NDMA’ 기준을 초과한 것으로 확인됐다.
해당 원료의약품들은 스페인 퀴미카 신테티카(Quimica Sintetica)社가 제조하여 ㈜팜스웰바이오가 수입한 1개 품목과 중국 지앙쑤 종방(Jiangsu Zhongbang)社가 제조한 명문제약㈜의 1개 품목이다.
최근 3년(2015~2017) 국내 전체 ‘발사르탄’ 원료의약품 시장에서 팜스웰바이오(스페인 퀴미카 신테티카)는 약 0.04%, 명문제약(중국 지앙쑤 종방)의 비중은 약 0.07%이다.
팜스웰바이오 ‘발사르탄’을 사용한 5개 완제의약품은 지난 7월 7일에 이미 판매중지됐다.
현재 해당 ‘발사르탄’ 원료의약품에서 ‘NDMA’가 기준을 초과한 원인 등에 대해 면밀히 검토를 진행하고 있다.
◆원료의약품 안전 관리 강화 및 복용 환자 영향 평가
식약처는 원료의약품 불순물 관리를 강화하기 위해 원료의약품에 대한 전반적인 안전관리 개선 방안을 마련, 시행한다는 계획이다.
앞으로 원료의약품 등록 제도를 개선하여 의약품에 포함될 수 있는 불순물에 대한 자체 관리를 의무화하고, 해외제조소 등록제 및 실사 근거를 법제화하여 관리 체계를 강화한다.
또 제약사가 ‘발사르탄’의 ‘NDMA’ 기준 적합 여부를 확인한 후 적합한 원료만 사용할 수 있도록 하여 안전한 제품만 유통될 수 있도록 조치한다는 계획이다.
지난 8월 6일 발표 후 ‘발사르탄’의 ’NDMA’ 함량 분석 결과, 건강보험심사평가원이 보유한 환자 정보 등을 바탕으로 NDMA 검출 제품을 복용했던 환자들에 대한 영향 평가를 진행하고 있으며, 이후 그 결과를 공개할 예정이다.
◆판매중지 등 조치된 발사르탄 의약품 교환 방법
보건복지부(장관 박능후)는 식약처 발표에 따라 이번에 판매 중지된 의약품을 처방 받은 환자 분들에 대한 조치방안을 마련하여 운영한다고 밝혔다.
해당 의약품 처방·조제한 의료기관은 805개소(병원 311, 약국 494)이며, 해당 의약품을 복용 중인 환자 수는 총 4,048명(8.23일 0시 기준)이다.
앞으로 해당 의약품이 의료기관에서 처방되지 않도록 8월 23일 0시부터 건강보험심사평가원의 의약품안전사용서비스(DUR) 시스템을 통해 처방·조제를 차단하고, 건강보험 급여 적용도 정지다.
이번에 문제된 의약품을 처방 받은 환자들은 종전에 처방을 받은 요양기관에 방문해야 1회에 한해 환자 본인부담금 없이 문제가 없는 다른 고혈압 치료제로 재처방, 재조제를 받을 수 있다.
의료기관을 방문할 수 없어 종전에 조제를 받았던 약국에 직접 방문하는 경우에도 의약품 교환이 가능하다.
재처방·재조제시 동일 ‘발사르탄’ 성분 내 교환뿐만 아니라 ‘발사르탄’ 성분에서 다른 성분의 고혈압 치료제로도 교환할 수 있다(단, 약국에서 약사법에 따라 대체조제 하는 경우는 제외).
기존에 처방을 받은 병·의원 또는 약국에서 의약품의 재처방·재조제시 1회에 한해 환자 본인이 부담해야하는 본인부담금이 발생하지 않는다.
복지부는 건강보험심사평가원에서 복용환자 명단을 파악하여 처방을 받은 병·의원 등 의료기관에 제공하면 의료기관에서는 ‘요양기관업무포털’에 접속, 해당 의약품을 처방·조제 받은 환자명단을 확인한 후 환자들에게 개별적으로 연락해 ①현재 복용 중인 의약품이 판매중지대상임을 알리고, ②우선적으로 진료 받았던 의료기관을 방문하여 처방을 변경하거나, 부득이한 경우에는 조제 받은 약국을 방문하도록 안내한다는 계획이다.
식약처는 “이번 조치 대상 의약품을 복용 중인 환자분들은 임의로 복용을 중단하지 말고 해당 의약품을 처방받은 병?의원 등 의료기관에 상담을 거쳐 재처방 등을 받을 것”을 당부했다.
◆대한고혈압학회 입장은?
불순물 함유 발사르탄에 대해 대한고혈압학회(회장 신길자, 이사장 조명찬)는 해당 발사르탄 제제를 처방받은 환자분들에게 다음과 같이 권고했다.
▲조치 대상 발사르탄 제제이더라도 혈압약을 임의로 중단하지 말아야 한다. 특히 고위험군이나 심혈관질환자는 혈압약 중단에 따른 뇌졸중, 심근경색 혹은 심부전 발생 등의 심각한 문제가 발생할 수 있다.
▲해당 의약품을 처방받은 병·의원에서 재처방 혹은 처방변경을 받고, 필요하다면 담당의사와 상담하라는 입장이다.
대한고혈압학회는 “이러한 문제발생의 원인, 재발방지 및 대책에 대해 관련 기관 혹은 전문학술단체와 논의하여 향후 국민과 정부에 정확한 정보와 가이드라인을 제시하는 노력을 기울이겠다”고 강조했다.
한편 고혈압은 30세 이상 성인의 29.1%가 가지고 있는 국민병으로 질병부담과 의료비를 포함한 사회경제적 부담이 매우 크기 때문에 고혈압의 치료와 조절 등 적절한 관리가 중요하다.
대한고혈압학회에서 올해 발표한 고혈압 팩트시트에 따르면 우리나라의 고혈압 유병자 수는 지속적으로 증가해 1,100만명을 넘었으며, 고혈압 치료제를 처방 받은 사람은 820만명으로 계속 증가하고 있고 꾸준히 고혈압 치료제를 처방 받은 사람도 570만명이나 된다.
고혈압 치료제 중 칼슘채널차단제가 그동안 가장 널리 사용되어 왔지만 최근에는 발사르탄(valsartan) 같은 안지오텐신수용체차단제(ARB)가 가장 많이 사용되고 있다. 많은 국민이 장기간 또는 평생 복용해야 하는 고혈압 치료제의 안전성은 아무리 강조하고 지나침이 없고 보건당국에서는 엄격한 관리기준을 세워 확인하고 정보를 제공해야 한다는 것이 대한고혈압학회의 입장이다.
잠정 판매중지 및 처방 제한 관련 제품 목록은 인터넷 포털사이트 ‘네이버’ 등에서 ‘고혈압약, 발사르탄, 고혈압치료제, NDMA’ 단어 검색을 통해 확인할 수 있다.
(표)발사르탄 관련 추가 검사 결과
다른 곳에 퍼가실 때는 아래 고유 링크 주소를 출처로 사용해주세요.
 http://www.medicalworldnews.co.kr/news/view.php?idx=1510927109
http://www.medicalworldnews.co.kr/news/view.php?idx=1510927109