식품의약품안전처(처장 류영진)가 ‘N-니트로소디메틸아민(NDMA)’ 발생할 가능성이 높은 제조공정을 시작으로 모든 발사르탄(52개사, 86개 품목)에 대하여 순차적으로 자료 검토 및 수거검사를 진행하고 있다고 밝혔다.
우선 중국 제지앙화하이社와 유사한 제조공정으로 제조된 발사르탄(24개사, 31개 품목)들 중에서 대표성이 있는 품목을 대상으로 수거·검사한 결과, NDMA 잠정 관리 기준(0.3ppm)을 초과한 제품은 없는 것으로 조사됐다.
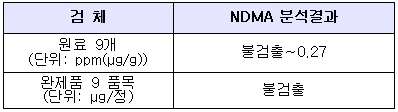
(표)중국 화하이社 발사르탄 관련 수거 검사 결과
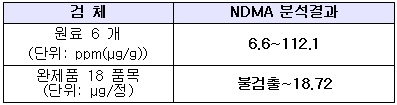
(표)중국 화하이社 발사르탄과 유사 공정 관련 수거 검사 결과
또 화하이社와 제조공정이 다르거나 추가 확인이 필요한 발사르탄(31개사, 46품목)에 대해서는 자료 검토 및 수거·검사를 진행 중이며, 화하이社가 제조한 발사르탄 외 다른 원료의약품에 대해서도 조사를 진행 중이다.
한편 식약처는 향후 발사르탄 내 불순물인 ‘NDMA’ 관리를 강화하기 위하여 관련 규정 개정을 통해 기준을 0.3ppm 이하로 설정하여 관리한다고 밝혔다.
이 기준은 국제의약품규제조화위원회(ICH)가 권고하고 있는 가이드라인(ICH M7: International Council for Harmonisation Mutagenic 7, 의약품 중 유전독성 불순물의 평가 및 관리 가이드라인), 국내외 자료 및 전문가 자문 등을 검토하여 설정됐다.
식약처 공식 자문기구인 중앙약사심의위원회도 유럽의약품안전청(EMA) 등 외국 기관에서도 잠정적으로 동일한 기준을 적용하고 있고, NDMA 위해성을 고려해 볼 때 해당 기준 설정이 타당하다고 자문했다.
이번에 설정된 NDMA 기준(0.3ppm)은 향후 ‘발사르탄’ 및 발사르탄이 함유된 모든 완제의약품에 적용되며, 기준을 초과 시 해당 제품은 회수 조치된다.
다른 곳에 퍼가실 때는 아래 고유 링크 주소를 출처로 사용해주세요.
 http://www.medicalworldnews.co.kr/news/view.php?idx=1510926880
http://www.medicalworldnews.co.kr/news/view.php?idx=1510926880